プロドラッグ型クルクミン注射製剤の抗腫瘍効果及び治療標的の包括的な解析
京都大学医学研究科 腫瘍薬物治療学講座 金井雅史 准教授、 同研究科 血液内科学講座 白川康太郎 助教、 同大学院薬学研究科 掛谷秀昭 教授、
株式会社セラバイオファーマらの共同研究グループは、
経口投与では吸収されにくいというクルクミン原末の問題点を克服した安全性の高い水溶性プロドラッグ型クルクミン(TBP1901)が、
既存の抗がん薬に抵抗性を示す多発性骨髄腫を移植したマウスモデルにおいて、 安全性に優れ顕著な抗腫瘍効果を示すことを明らかにしました。
ショウガ科のウコンに含まれるポリフェノール化合物であるクルクミンは、 古くより香辛料や着色料として広く用いられてきました。
クルクミンは基礎研究で様々ながん種に対し抗腫瘍効果を発揮することが証明されており、 抗がん薬としての開発が期待されてきました。 しかし、
クルクミン原末をそのまま経口摂取しても多くは腸管で吸収されないために、 その抗がん作用を引き出すのに十分な血中濃度を得ることはできませんでした。
そこで研究グループは、 クルクミンの生物学的利用能(バイオアベイラビリティー)※1の向上のために精力的な研究を行った結果、 生体内において、
クルクミンモノグルクロニド(CMG)がクルクミンのプロドラッグとして利用でき、
既存の抗がん薬(オキサリプラチン)に抵抗性を示す大腸癌モデルに対し優れた抗腫瘍効果を発揮することを報告しています文献1。
さらにクルクミンモノグルクロニド・ナトリウム塩とすることで、
化合物として安定性の高い水溶性プロドラッグ型クルクミン(TBP1901)の製造方法を確立させました。
今回標準治療薬(ボルテゾミブ)に抵抗性を示す多発性骨髄腫マウスモデルを用いて、 TBP1901が体重減少等の副作用を伴うことなく、
顕著な抗腫瘍効果を発揮することを明らかにしました(右図)。 さらに生体内におけるTBP1901からクルクミンへの活性化にはβ-グルクロニダーゼ
(GUSB)と呼ばれる酵素が関与すること、
またCRISPR-Cas9スクリーニング※2という手法をもちいて活性本体であるクルクミンの標的について包括的な解析を行いました。
TBP1901の活性本体であるクルクミンは香辛料としても広く用いられている化合物であることから、 安全性の高い抗がん薬としての開発が期待されます。
本研究成果は、 2022年10月11日(現地時刻)に「European Journal of Pharmacology」のオンライン版に掲載されました。
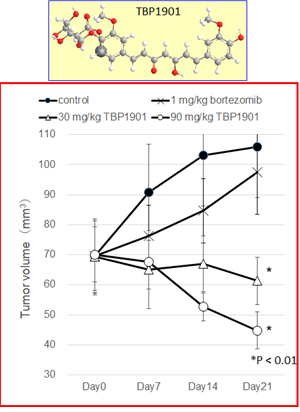
図 標準治療薬であるボルテゾミブ抵抗性の多発性骨髄腫細胞株を用いたマウスモデル。 TBP1901投与群では腫瘍は著明に縮小。
1.背景
ショウガ科のウコンに含まれるポリフェノール化合物クルクミンは、 古くより香辛料や着色料として広く用いられてきました。
クルクミンは基礎研究で様々ながん種に対し抗腫瘍効果を発揮することが証明されており、 抗がん薬としての開発が期待されており、 現在も多くの研究が行われています。
しかしクルクミン原末をそのまま経口摂取しても多くは腸管で吸収されないために、 その抗がん作用を引き出すのに十分な血中濃度を得ることはできませんでした。
そこで研究グループは、 クルクミンの生物学的利用能(バイオアベイラビリティー)の向上のために精力的な研究を行った結果、 生体内において、
クルクミンモノグルクロニド(CMG)がクルクミンのプロドラッグとして利用できることを証明しています文献2。
プロドラッグとは、 生体内で代謝され活性代謝物となる薬剤です。 さらに、 大腸がんのマウスモデルを用いて、
クルクミンモノグルクロニドが大腸がんの標準治療薬であるオキサリプラチンより安全で優れた抗腫瘍効果を発揮することも明らかにしています。
クルクミンモノグルクロニド・ナトリウム塩とすることで、 化合物としての安定性が格段に向上して薬剤開発の点で有利であることから、 これをTBP1901と命名し、
抗がん薬としての臨床応用を目指した研究を京都大学発のベンチャー企業である株式会社セラバイオファーマ社と共同で行っています。
2.研究手法・成果
TBP1901を用いて、 以下の2つの点を明らかにすることを目的として研究を行いました。
1.生体内でTBP1901から活性本体であるクルクミンへの代謝に関与するメカニズムの解明
2.クルクミンの抗腫瘍効果に重要な標的をCRISPR-Cas9スクリーニングと呼ばれる新しい手法を用いることでの包括的な検討
今回、 TBP1901から活性本体であるクルクミンへの生体内での代謝にはβ-グルクロニダーゼ (GUSB) と呼ばれる酵素が不可欠であること、
またこのGUSB活性は特に骨髄で高く、 TBP1901からクルクミンへの変換効率も骨髄で優れていることを明らかにしました。
骨髄で増殖するがん種への臨床応用がその薬物動態上の特性を活かすことができると考え、 多発性骨髄腫でTBP1901の薬効を評価したところ、
標準治療薬であるボルテゾミブに対して抵抗性を示す多発性骨髄腫のマウスモデルに対してもTBP1901は体重減少等の副作用を伴うことなく、
顕著な抗腫瘍効果を示しました。
一方、 CRISPR-Cas9スクリーニングの手法を用いてクルクミンの標的を包括的に検討したところ、 NF-κB経路や活性酸素種 (ROS)
産生に関与する遺伝子群が上位にランクされました。 クルクミンがこれらの経路を標的とすることは複数のグループから報告されていましたが、
CRISPR-Cas9スクリーニングの手法を用いた包括的な検討は本研究が初めてです。
3.波及効果、 今後の予定
今回TBP1901が生体内においてGUSBで活性体であるクルクミンに代謝されること、 さらに骨髄ではGUSB活性が高く、
クルクミンへの変換効率が高いことを明らかにしました。 またクルクミンは多くの標的を有する(マルチターゲット)ことが基礎研究で報告されていますが、
CRISPR-Cas9スクリーニングの結果から、 クルクミンの抗腫瘍効果のメカニズムとしてはNF-B経路の抑制やROS産生が重要と考えられました。
クルクミンの抗腫瘍効果のメカニズムは既存の抗がん薬と異なりマルチターゲットという点でユニークであることから、
既存の抗がん薬に抵抗性を示すがん細胞に対しても抗腫瘍効果を発揮することができると考えられます。
TBP1901の活性本体であるクルクミンは香辛料としても広く用いられている化合物であることから、 安全性の高い抗がん薬としての開発が期待されます。
4.研究プロジェクトについて
本研究は、 京都大学大学院医学研究科、 京都大学大学院薬学研究科、 株式会社セラバイオファーマらとの共同研究であり、 一部、
文部科学省新学術領域研究(研究領域提案型)「化学コミュニケーションのフロンティア」(17H06401)の支援のもとに行なわれました。
<参考文献>
文献1. Curcumin β-D-glucuronide exhibits anti-tumor effects on
oxaliplatin-resistant colon cancer with less toxicity in vivo. Cancer Sci. 2020,
111:1785-1793.
文献2. Curcumin β-D-glucuronide plays an important role to keep high levels of
free-form curcumin in the blood. Biol. Pharm. Bull. 2017, 40: 1515-1524.
<用語解説>
※1 バイオアベイラビリティー:人体に投与された薬剤が、 どれだけ体内を循環しているかを示す指標です。
※2 CRISPR-Cas9スクリーニング:CRISPR-Cas9は2020年にノーベル化学賞を受賞した、 新しいゲノム編集技術です。
この手法を用いることにより薬物の標的を包括的に解析することが可能となりました。
<研究者のコメント>
クルクミンは香辛料としても使われている天然化合物です。 クルクミンが抗がん作用を有することは多くの基礎研究で証明されていますが、
経口投与では抗がん作用を発揮するのに十分な血中濃度が得られませんでした。 TBP1901は体内でクルクミンに変換されるプロドラッグ型の注射製剤であり、
安全性の高い新しい抗がん薬としての開発が期待できると考えています(金井雅史、 掛谷秀昭)。
<論文タイトルと著者>
タイトル:Pharmacologic characterization of TBP1901, a prodrug form of aglycone
curcumin, and CRISPR-Cas9 screen for therapeutic targets of aglycone
curcumin.(クルクミン注射製剤TBP1901の薬理学的特徴とCRISPR-Cas9スクリーニングの手法を用いた活性本体であるクルクミンの標的分子の包括的な検討)
著 者:Tomoyuki Abe, Yoshihito Horisawa, Osamu Kikuchi, Hitomi Ozawa-Umeta,
Atsuhiro Kishimoto, Yasuhiro Katsuura, Atsushi Imaizumi, Tadashi Hashimoto,
Kotaro Shirakawa, Akifumi Takaori-Kondo, Kosuke Yusa, Tadashi Asakura, Hideaki
Kakeya, Masashi Kanai
掲 載 誌:European Journal of Pharmacology DOI:
https://doi.org/10.1016/j.ejphar.2022.175321
<お問い合わせ先>
京都大学 総務部広報課国際広報室
TEL:075-753-5729 FAX:075-753-2094
E-mail: [email protected]
<参考図表>
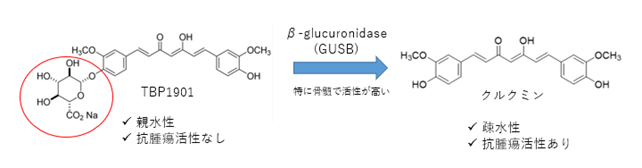
図1. TBP1901自身は抗腫瘍活性を有しないが、 親水性で静脈投与が容易である。 生体内に投与するとβ-glucuronidase (GUSB)
によってグルクロン酸抱合(赤丸)が外れて、 クルクミンに代謝され、 NF-κB経路の抑制や活性酸素種の産生を亢進させることにより抗腫瘍効果を発揮する。







ディスカッション
コメント一覧
まだ、コメントがありません